"Erwachsene nehmen eine Tablette, Kinder die Hälfte" - solche Dosierungsempfehlungen können schwere Folgen haben. Denn was Erwachsenen hilft, kann bei Kindern gefährliche Nebenwirkungen hervorrufen oder wirkungslos sein. Jahrzehntelang wurden Arzneimittel nur an Erwachsenen getestet und für diese zugelassen, weil der Markt für Kindermedikamente der Pharmabranche nicht lukrativ genug war.
Seit 2007 müssen Medikamente zwar auch an Kindern getestet werden, doch gelten solche Kinderstudien als schwierig, langwierig und teuer. Die Folge: Spezielle Arzneimittel für Kinder kommen nur sehr zögerlich auf den Markt.
Gerade für Frühgeborene gibt es kaum getestete Medikamente
Fast alle Arzneien, die im Brutkasten verwendet werden, stammen aus der Erwachsenenmedizin. Das bedeutet, dass jedes Frühchen zum Testfall wird. Professor Hubert Fahnenstich, Chefarzt des Lörracher Zentrums für Kinder- und Jugendmedizin erklärt: „Frühchen sind extrem empfindlich, haben ein unreifes Enzymsystem, um Medikamente zu verarbeiten. Wenn diese Kinder in einen kritischen Zustand geraten sollten, bekommen sie Medikamente, die Herz und Kreislauf stärken.
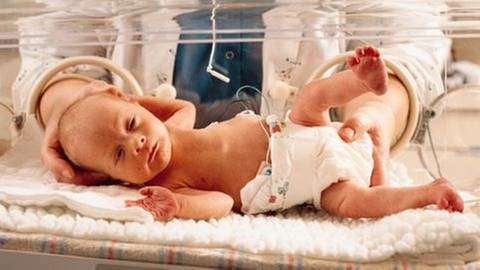
Je älter die Kinder sind, desto eher liegen zu den Medikamenten, die verwendet werden, Prüfungen vor. Je jünger, desto schwieriger wird es. Und da würde man sich häufiger wünschen, man hätte da mehr kontrollierte Studien.“
Jedes zweite Medikament, das Kinder erhalten, ist nur an Erwachsenen getestet
Professor Fred Zepp, Direktor des Mainzer Zentrums für Kinder- und Jugendmedizin, ist der Experte für Kindermedikamente bei der Deutschen Gesellschaft für Kinder- und Jugendmedizin. Er schätzt dass im ambulanten Bereich zwischen 20 und 30 Prozent Medikamente verabreicht werden, die nicht für Kinder geprüft wurden. Im Krankenhaus liegt die Rate noch deutlich höher. „Das hat damit zu tun, dass die Kinder, die dort betreut werden, oft schwerwiegender krank sind. Und am höchsten ist der Anteil an Medikamenten, die nie bei Kindern getestet wurden, in der Neugeborenen-Intensivmedizin. Dort sind es geschätzt 90 Prozent.“
Bei schweren und seltenen Krankheiten fehlen spezielle Kindermedikamente
Im Klinikalltag müssen Kinderärzte daher auf Medikamente zurückgreifen, die nur für Erwachsene zugelassen wurden. Dieses Verfahren wird „Off-Label-Use“ genannt: „Wenn ein Medikament nur an Erwachsenen untersucht wurde, dann kann man es eigentlich nicht an Menschen unter 18 Jahren einsetzen. Das heißt unter der Notwendigkeit, einem kranken Kind helfen zu müssen, sind Kinderärzte und Kinderärztinnen immer wieder der Situation ausgesetzt, Entscheidungen zu treffen, ohne auf eine solide wissenschaftliche Datenbasis bezüglich der Medikamente zurückgreifen zu können.“
Erwachsenenmedikamente auf Kinder runterzurechnen ist schwierig
Das große Problem dabei ist, die richtige Dosierung zu finden. Einfach nur die halbe Dosis geht nicht. Denn Kinder befinden sich im Wachstum. Die Dosis muss individuell ermittelt werden. Kinderärzte müssen aus einer Kombination von Gewicht, Alter und Entwicklungsstand des Kindes heraus abschätzen, welche Dosierung sinnvoll ist.

Über Nebenwirkungen bei Kindern ist nichts bekannt
Viele Kinder reagieren mit unerwünschten Begleiterscheinungen, mit Kopfschmerzen, Schwindelgefühlen bis hin zu schweren Komplikationen. Im Klinikalltag bleibt den Kinderärzten aber oft keine andere Wahl. Sie müssen ihre kleinen Patienten behandeln – vor allem, wenn sie lebensgefährlich erkrankt sind. Eine off-label“-Behandlung ist dann nicht nur eine Zitterpartie, die Kinderärzte bewegen sich auch in einer rechtlichen Grauzone. In heiklen Fällen müssen sie deshalb immer die Zustimmung der Eltern einholen.
Sichere Medikamente für Kinder werden dringend gebraucht
Um die Entwicklung von Medikamenten für die Kleinen voranzutreiben, hat die Europäische Union 2007 eine neue Regelung erlassen. Diese EU-Kinderverordnung schreibt vor, dass die Zulassungsunterlagen für ein neues Medikament auch ein pädiatrisches Prüfkonzept enthalten müssen – also den Plan für eine Kinderstudie. Als Anreiz dafür erhalten die Hersteller Patentverlängerungen. Wird ein neuer Wirkstoff an Kindern getestet, wird das Patent um ein halbes Jahr verlängert.
Wird ein alter Wirkstoff nachgetestet, ist das Mittel zehn Jahre lang geschützt. Doch zehn Jahre nach der EU-Kinderverordnung fällt die Bilanz ernüchternd aus. Tatsächlich sind nur 260 neue Kinderarzneimittel auf den Markt gekommen. In etwa so viele wie in der Dekade zuvor. Ein enttäuschendes Ergebnis.
Warum gibt es so wenig Kinderstudien?
• Viele Kinderstudien scheitern schon daran, dass es nicht genügend Probanden gibt – beklagt der Verband der Arzneimittelhersteller: Nur 20 Prozent der Bevölkerung sind im Alter zwischen Neugeborenen und 18 Jahren. Hinzu kommt, dass diese Bevölkerungsgruppe bis zu 18 Jahren, nochmals unterteilt werden muss in fünf unterschiedliche Altersgruppen: nämlich Frühgeborene, Neugeborene, Säuglinge Kinder und Jugendliche. So dass die Zahl potentieller Kandidaten für solche klinische Studie immer kleiner wird.
• Kinderstudien sind an hohe Auflagen geknüpft und werden streng überwacht. Klinische Studien dürfen nur an kranken Kindern vorgenommen werden, damit die Kinder unmittelbar von den klinischen Prüfungen profitieren. Das ist anders als bei Erwachsenen, da können auch gesunde Erwachsene an Erprobungsstudien teilnehmen - bei Kindern geht das nicht.
• Der Verband der Arzneimittelhersteller erklärt: Die Neuentwicklung eines Arzneimittels kostet etwa 1 bis 1,3 Milliarden Euro. Die spezifischen Untersuchungen, ob dieses Arzneimittel für Kinder angewendet werden kann, kosten etwa 20 Millionen Euro mehr. Diese Kosten müssen wieder reinkommen – doch der Absatzmarkt für ein Kindermedikament ist viel kleiner als der für Erwachsene. Deshalb stellen viele Pharmaunternehmen diese Studien zurück.
Noch mehr Geduld ist bei der Neuzulassung von altbekannten und bereits an Erwachsenen geprüften Medikamenten gefordert. Die Pharmaindustrie soll diese Mittel freiwillig in Kinderstudien nachtesten. Als „Belohnung“ dafür gibt es einen zehnjährigen Patentschutz. Wenn sich ein Wirkstoff bei Minderjährigen bewährt, dann kann er in kindgemäßen Säften oder Tabletten hergestellt werden.
Kinderärzte fordern mehr Nachzulassungen von bekannten Wirkstoffen für Kinder
An alten Wirkstoffen sind die Kinderärzte besonders interessiert. Denn im Klinikalltag setzen sie diese Medikamente regelmäßig „off-label“ ein. Doch die Pharmahersteller halten diese Nachzulassungen für ein Verlustgeschäft. Grund dafür ist die mangelnde Kostenerstattung. Denn für Wirkstoffe, deren Patent bereits abgelaufen ist, haben die Krankenkassen Festbeträge eingeführt.
Für ein Kindermedikament gibt es deshalb in der Regel nur den gleichen Erstattungsbeitrag wie für das Erwachsenenpräparat. Die Herstellung eines kinderfreundlichen Saftes ist aber wesentlich teurer und aufwendiger als die schlichten Erwachsenentabletten.

Schweizer Computermodell hilft Kinderärzten bei der Berechnung von kindgerechter Dosierung
In der Schweiz hat ein Mäzen 15 Millionen Franken gestiftet, damit eine interdisziplinäre Forschungsgruppe an virtuellen Lösungen arbeiten kann, ohne dass ein Kind dafür getestet werden muss: Die Basler Spezialisten entwickeln Computermodelle aus bereits vorhandenen Daten und entwickeln daraus Simulationen. Mit Hilfe der errechneten Dosierung können die Basler Forscher einen Erfolg versprechenden Prüfplan für eine Kinderstudie erstellen – das langwierige Experimentieren mit verschiedenen Dosis-Varianten fällt weg.
Zudem entwickelt die Basler Forschergruppe spezielle Apps mit Dosierungsempfehlungen. Damit können Kinderärzte die optimale Dosierung eines Erwachsenenmedikaments direkt auf ihrem Smartphone abrufen. Solche computergestützten Hilfsmittel werden in der Kindermedizin künftig immer wichtiger werden. Alle Experten sind sich nämlich einig: bis ausreichend Medikamente für Kinder zur Verfügung stehen, werden noch Jahre, wenn nicht Jahrzehnte vergehen. Bis dahin müssen Kinderärzte ihre kleinen Patienten weiterhin „off-label“ behandeln.
SWR 2018